标准规范下载简介
在线阅读
中华人民共和国国家标准
医药工艺用水系统设计规范
Code for design of pharmaceutical process water system
GB 50913-2013
主编部门:中国医药工程设计协会
批准部门:中华人民共和国住房和城乡建设部
施行日期:2014年5月1日
中华人民共和国住房和城乡建设部公告
第150号
住房城乡建设部关于发布国家标准《医药工艺用水系统设计规范》的公告
本规范由我部标准定额研究所组织中国计划出版社出版发行。
中华人民共和国住房和城乡建设部
2013年9月6日
前言
本规范是根据住房和城乡建设部《关于印发<2008年工程建设标准规范制订、修订计划(第二批)>的通知》(建标[2008]105号)的要求,由中国医药集团联合工程有限公司会同有关单位共同编制完成的。本规范在编制过程中,编制组经广泛调查研究,认真总结医药工艺用水在工程实践中的经验,参考有关国际标准,并广泛征求意见,最后经审查定稿。
本规范共分8章和3个附录,主要内容包括:总则、术语和符号、水质、工艺系统设计、管道、站房、建筑与结构、公用工程等。
本规范中以黑体字标志的条文为强制性条文,必须严格执行。
本规范由住房和城乡建设部负责管理和对强制性条文的解释,由中国医药工程设计协会负责日常管理,由中国医药集团联合工程有限公司负责具体技术内容的解释。本规范在执行过程中如有意见或建议,请寄送至中国医药集团联合工程有限公司(地址:湖北省武汉市武昌区黄鹂路25号,邮政编码:430077),以供今后修订时参考。
本规范主编单位、参编单位、参加单位、主要起草人和主要审 查人:
主编单位:中国医药集团联合工程有限公司
参编单位:中国石化集团上海工程有限公司
中国医药集团重庆医药设计院
阿法拉伐(中国)有限公司
参加单位:上海朗脉科技有限公司
上海奥星制药技术装备有限公司
倍世水技术(上海)有限公司
主要起草人:刘元 张长银 张奇 许继辉 杨丽敏 李忠德 冯庆 叶萍 刘艳艳 李云 陈功平 李陈江 缪晡 杨军 谭建国 卢浩荣 吴霞 陶晓明 王朋良 郑程灿 陈国笋 周继军 张功臣 易军 陆明海 奥利弗瓦克
主要审查人:马立新 甘长霖 李波 宋丽萍 王晓东 许小球 郭珍珍 华永康 林辉 沙琦 胡征 温利明 范平浩 孙桂芝 李青 甘平
1 总则
1.0.1 为在医药工艺用水系统设计中贯彻执行《药品生产质量管理规范》(GMP),做到技术先进、经济合理、运行可靠、确保质量,满足环境保护和节约能源的要求,制定本规范。
1.0.2 本规范适用于新建、改建和扩建的医药工艺用水系统的设计。
1.0.3 医药工艺用水系统的设计应为施工安装、维护管理、检修和运行创造必要的条件。
1.0.4 医药工艺用水系统的设计,除应符合本规范外,尚应符合国家现行有关标准的规定。
.
2 术语和符号
2.1 术语
2.1.1 医药工艺用水 pharmaceutical process water
医药生产工艺过程中使用的水,包括生活饮用水、纯化水、注射用水。
2.1.2 原水 raw water
进入医药工艺用水生产装置或设备有待进一步处理的水。
2.1.3 生活饮用水 drinking water
指供人生活的饮水和生活用水,简称饮用水。
2.1.4 纯化水 purified water
蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的医药工艺用水,不含任何添加剂。
2.1.5 注射用水 water for injection
纯化水经蒸馏所得的水。
2.1.6 分配系统 distribution system
从产生或供应的地方到使用点配送工艺用水的整套系统。
2.1.7 站房 station building
制备医药工艺用水的建筑物的总称。
2.1.8 确认 qualification
证明厂房、设施、设备能正确运行并可达到预期结果的一系列活动。
2.1.9 纯蒸汽 pure steam
用纯化水或注射用水经蒸汽发生器或多效蒸馏水机制得的蒸汽。
2.1.10 死角 dead leg
在医药工艺用水系统中可能导致工艺用水污染的滞流区域/点。
2.1.11 卫生 hygienic
设备或管路系统的设计、材质和操作符合其清洁维护要求,由设备或管路系统生产出的工艺用水不会对人类和生物健康产生不利的影响。
2.2 符号
2.2.1 设计流量:
Q——管路设计流量;
Qmax——所有用水点的累积最大出水量;
Qb——回水流量。
2.2.2 管径确定:
d——管道内直径;
Vf——工艺用水的体积流量;
u——工艺用水的平均流速;
W——工艺用水的质量流量;
ρ——工艺用水的密度。
2.2.3 压力损失计算:
△Pf——管道总摩擦压力降;
λ——摩擦系数;
L——管道长度;
D——管道内直径;
K——管件、阀门等阻力系数;
△Ps——静压力降;
Z1、Z2——分别为管道系统始端、终端的标高;
g——重力加速度;
△PN——速度压力降;
u1、u2——分别为管道系统始端、终端的流体流速;
△P——管道系统总压力降;
k——裕度系数;
△Pfz——直管段摩擦压力降;
△PK——流体经管件或阀门的压力降;
△Pkf——阀门的局部压力降;
Kv——阀门的流量系数。
3 水质
3.0.1 医药工艺用水的水质应符合生产工艺要求的质量标准。
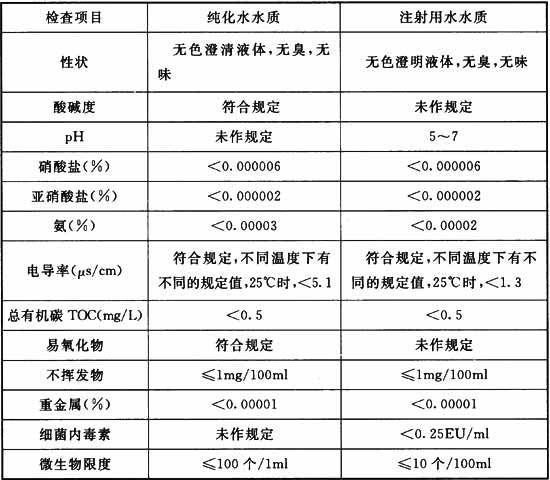
3.0.2 医药工艺用水的水质应符合下列要求:
1 饮用水水质应符合现行国家标准《生活饮用水卫生标准》GB 5749的有关规定。
2 纯化水水质应符合表3.0.2的规定和药品生产要求。
3 注射用水水质应符合表3.0.2的规定和药品生产要求。
表3.0.2 纯化水和注射用水检查项目
.
4 工艺系统设计
4.1 一般规定
4.1.1 水源应保证连续供应所需的水量和稳定的水质。
4.1.2 制水工艺流程应根据原水水质、生产工艺对工艺用水的水质要求进行选择。
4.1.3 工艺用水系统应符合下列要求:
1 应满足经济、适用的要求。
2 应满足布置紧凑、操作简便、安全可靠的要求。
3 应满足节水、节能和环境保护的要求。
4.1.4 工艺用水系统的设计能力应根据用水量和生产负荷确定。
4.2 工艺用水制备
4.2.1 饮用水可采用混凝、沉淀、澄清、过滤、软化、消毒、去离子、沉淀、减少特定的无机/有机物等物理、化学和物理化学的方法制备。
4.2.2 纯化水制备的原水应采用饮用水,并应采用合适的单元操作或组合的方法制备,如蒸馏、离子交换、反渗透、过滤等。
4.2.3 注射用水的水源应以纯化水为水源,并应采用蒸馏方法制备。
4.3 设备
4.3.1 预处理设备应根据原水水质配备,出水水质应符合后续处理设备的进水要求。
4.3.2 蒸馏水机应符合现行行业标准《多效蒸馏水机》JB/T 20030及《热压式蒸馏水机》JB 20029的有关规定。
4.3.3 多效蒸馏水机应设置原水泵。
4.3.4 纯化水储罐和注射用水储罐的设计和选型,应符合下列要求:
1 纯化水储罐应采用无毒、耐腐蚀材料制造。注射用水储罐应采用优质低碳不锈钢制造。
2 纯化水储罐和注射用水储罐的罐盖、人孔和罐底阀门等零部件应设计为卫生连接的方式,并应便于拆卸和清洗。可拆卸零部件与罐体之间的密封材料应无毒、无析出物、耐高温、无脱落物。
3 罐体结构件不得有裂纹、开焊和变形,内壁表面应光滑平整、无死角。
4 纯化水储罐和注射用水储罐的最低处应设置排放口,排水管路不应出现使水滞留的部位。储罐应设置液位计量装置,液位计量装置不得有对水质产生污染的风险。除采用臭氧连续灭菌的储罐外,再循环系统储罐顶部应设置喷淋装置,喷淋装置的设置应避免形成能滋生微生物的死角。
5 储罐的通气口应安装不脱落纤维的0.22μm疏水性通气过滤器,并应能满足输水泵以最大流量注入水或在高温消毒的循环水中体积收缩的情况下有效地卸放负压的要求。
6 当纯化水储罐和注射用水储罐采用灭菌时,储罐应按压力容器设计,并应达到卫生设计标准。对需热贮存的注射用水储罐罐体应保温,保温层表面应平整、光洁。
4.3.5 储罐的大小应能满足各种用水条件下的储水量要求。纯化水储罐和注射用水储罐的容量应符合下列要求:
1 贮水量的大小应符合下列要求:
1)应满足系统循环时蒸馏水机连续运行的要求;
2)满足用水点的平行以及顺序的各种加工要求;
3)在用水高峰时期,储罐内的水位不应低于输送泵净正吸水压头所要求的水位,并确保有足够的水流流过所有的供水点和回水管道。
2 应满足在制水设备出现故障或因设备消毒或再生循环而停产的情况下提供短期储备用水的要求。在确定储罐的容量时,应能够保证提供生产一个批次产品或者一个工作周期或其他合理需求的一段时间的用水。
4.3.6 纯化水和注射用水输送泵应采用不锈钢卫生泵、卫生卡箍作连接件。泵所有的润湿零部件应采用优质低碳不锈钢材质加工,泵外壳底部应能完全排除积水,泵出水口宜设置为45°。当采用双端面机械密封时,纯化水输送泵应采用纯化水润滑,注射用水输送泵应采用注射用水润滑。
4.3.7 注射用水输送泵提供的扬程和流量应确保水在输送系统中保持湍流。
4.3.8 过滤器的设置应符合下列要求:
1 过滤器的大小和材质应根据水的流量和水质确定,应对过滤系统内水压力进行监控。
2 在纯化水储罐出水口、分配输送管路不宜使用过滤器,在注射用水储罐出水口、分配输送管路不应使用过滤器。
4.3.9 换热器应按卫生要求设计,应采用优质低碳不锈钢制造。换热器不应出现使水滞留和不易清洁的部位。
4.4 工艺用水的分配输送
4.4.1 饮用水系统应设计成单向的保持持续正压的分配系统。
4.4.2 纯化水、注射用水的分配输送应有防止微生物滋生和污染的措施。
4.4.3 纯化水宜采用循环输送。循环输送管路应符合下列要求:
1 循环供水流速宜大于1.5m/s。
2 循环回水流速不宜小于1.0m/s,循环回水流量宜大于泵出口流量的50%。
3 支管长度不宜大于支管管径的3倍。
4.4.4 注射用水应采用循环输送。循环输送管路应符合下列要求:
1 宜采用70℃以上保温循环。
2 循环供水流速宜大于1.5m/s。
3 循环回水流速不应小于1.0m/s。
4 循环回水流量宜大于泵出口流量的50%。
5 支管长度不宜大于支管管径的3倍。
4.4.5 纯化水、注射用水可根据需要采用不同的循环方式确保纯化水、注射用水水质和使用要求。纯化水、注射用水宜采用单管循环输送,并应符合下列要求:
1 不含管道弯曲、弯头等的总长度应小于400m。
2 循环供水管路的直径DN不宜大于65mm。
3 当不能满足本条第1款、第2款的要求时,纯化水、注射用水的分配输送管路应采用双管循环输送或二次分配系统循环输送。
4.5 纯化水、注射用水系统的清洗、消毒和灭菌
4.5.1 预处理设备应根据运行和维护的要求设置清洗、消毒或灭菌措施。
4.5.2 纯化水储罐和输送系统应设置清洗、消毒设施。
4.5.3 注射用水储罐和输送系统应设置在位清洗、在位灭菌设施。
4.5.4 消毒灭菌措施应符合下列规定:
1 选用紫外线消毒时,紫外线有效剂量不应低于40mJ/cm²,紫外线消毒设备应符合现行国家标准《城市给排水紫外线消毒设备》GB/T 19837的规定。紫外灯应有计时器和照度计。
2 采用臭氧消毒时,宜采用紫外线照射除去臭氧。
3 根据季节变化,消毒方法可组合使用。
4.6 纯化水、注射用水的检测和控制
4.6.1 直接应用于药品生产某个阶段或作为原水生产纯化水的饮用水应定期检查。
4.6.2 消毒灭菌设备应安全可靠。
4.6.3 纯化水和注射用水系统的工艺参数应进行监控,并应按取样标准操作程序规定设置取样口检测水质。纯化水和注射用水在线检测系统应具备水质超标时程序报警功能。
4.6.4 纯化水系统宜安装流量、压力、温度、电导率等检测仪表,同时应根据水质要求配置水样的物理、化学和微生物污染等离线检测设备。注射用水系统应安装流量、压力、温度、电导率和总有机碳等检测仪表,同时应根据水质要求配置水样的物理、化学和微生物污染等离线检测设备。
4.6.5 纯化水和注射用水系统宜设自动化控制系统,并应具有手动控制功能。控制系统应运行安全可靠,应设置故障停机、故障报警装置。
4.6.6 纯化水和注射用水控制系统应有各设备运行状态和系统运行状态指示或显示,可按工艺要求按设定的程序进行自动运行。
4.6.7 纯化水和注射用水控制系统宜能显示重要运行参数,并宜设定监测指标的警戒限度与纠偏限度。
4.6.8 纯化水和注射用水控制系统应对缺水、过压、过流、过热、不合格水排放等有保护功能,并应根据反馈信号进行相应控制、协调系统的运行。
4.6.9 需要安装在工艺用水系统上的压力、温度及其他仪表,应满足卫生及在位清洗、在位灭菌要求。
4.7 纯蒸汽制备及输送
4.7.1 纯蒸汽应采用纯化水或注射用水经纯蒸汽发生器或多效蒸馏水机制备。
4.7.2 纯蒸汽分配系统应避免死角和冷凝水的积聚,安全阀、疏水器设置应合理。用于纯蒸汽的疏水器应为卫生设计、自行排水。
4.7.3 纯蒸汽输送应采用优质不锈钢或优质低碳不锈钢管道。
4.7.4 纯蒸汽流速宜小于25m/s,最大不得超过37m/s。纯蒸汽的凝水应排至单独的排水系统中。
.
5 管 道
5.1 一般规定
5.1.1 管道的设计应符合下列要求:
1 纯化水、注射用水管路系统宜避免死角、盲管。
2 管道布置设计应便于操作、安装及维护。
5.1.2 纯化水、注射用水制备系统宜预留清洗口,清洗口宜设在站房。
5.1.3 水平管道应有0.5%~1%的坡度,管路系统的排放管道应设置排放阀,排放管不应直接通向室外大气,应与地漏等保持空气阻断。
5.1.4 工艺用水管道宜布置在技术夹层或技术夹道内。引入洁净室(区)的管道当需要拆卸时宜明敷。
5.1.5 管道布置应确保工艺用水系统的独立性,不同水质的管路间应无交叉污染的风险。
5.1.6 用水点阀门应就近连接至设备。
5.2 管道的材质、阀门和附件
5.2.1 管道、管件等材料应在规定的使用压力和温度下具有足够的机械强度和耐腐蚀性能。
5.2.2 用于饮用水的输送管道、管件等的材料,宜选用不生锈、无腐蚀、无渗漏、无结垢的材料。
5.2.3 用于纯化水的输送管道、管件等的材料,应选用无毒、耐腐蚀的材料,宜选用内壁抛光的优质不锈钢材料或其他不污染纯化水的材料。
5.2.4 用于注射用水的输送管道、管件等的材料,应选用内壁抛光的优质低碳不锈钢材料或其他不污染注射用水的材料。
5.2.5 纯化水管道上的阀门应采用与连接的管道相适应的材料,管道上阀门应采用焊接或卡箍连接,不应采用螺纹连接,管道与法兰连接时应对齐,垫片内圈应与管道内壁等径,垫片应选用耐高温、不反应、不脱落、无析出物产生的材料。
5.2.6 注射用水管道上的阀门应采用焊接或卡箍连接的优质低碳不锈钢隔膜阀。
5.2.7 纯化水和注射用水系统管道上需要安装压力、温度及变送器等仪表时,应在管路上预留异径三通或等径三通接装仪表。
5.3 管径确定和压力损失计算
5.3.1 管径应根据工艺用水的流量、流速及管道允许的压力损失等确定。
5.3.2 工艺用水循环供水管路的直径应符合本规范第4.4.4条的规定。
5.3.3 工艺用水管径的确定应符合下列规定:
1 工艺用水管道的内径可按下式计算:
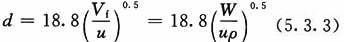
式中:d——管道内直径(mm);
Vf——工艺用水的体积流量(m³/h);
u——工艺用水的平均流速(m/s);
W——工艺用水的质量流量(kg/h);
ρ——工艺用水的密度(kg/m³)。
2 应按公式(5.3.3)计算得到的管道内径调整为实际内径,并应最后复核实际平均流速。
3 应以实际的管内径与平均流速核算管道压力损失,并应确认选用管径。管道压力损失不满足要求时,应重新计算。
5.3.4 管道平均流速不应超出1m/s~3m/s的流速允许范围。
5.3.5 工艺用水管道总压力损失应为管道摩擦压力降、静压力降以及速度压力降之和,并应计入适当的裕度,同时应符合下列要求:
1 摩擦压力降可按下式计算:
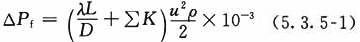
式中:△Pf——管道总摩擦压力降(kPa);
λ——摩擦系数,无因次;
L——管道长度(m);
D——管道内直径(m);
∑K——管件、阀门等阻力系数之和,无因次;
u——工艺用水的平均流速(m/s);
ρ——工艺用水的密度(kg/m³)。
2 静压力降可按下式计算:
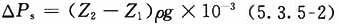
式中:△Ps——静压力降(kPa);
Z1、Z2——分别为管道系统始端、终端的标高(m);
g——重力加速度,9.81 m/s²。
3 速度压力降可按下式计算:
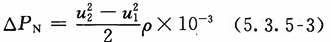
式中:△PN——速度压力降(kPa);
U1、U2——分别为管道系统始端、终端的工艺用水流速(m/s)。
4 管道系统总压力降可按下式计算:
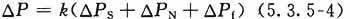
式中:△P——管道系统总压力降(kPa);
△Ps——静压力降(kPa);
△PN——速度压力降(kPa);
△Pf——摩擦压
k——裕度系数,取1.2~1.3。
5.3.6 管道允许的压力损失不宜超过0.05MPa/100m。
5.4 管道安装
5.4.1 不锈钢管道安装前,应确保每一个焊接点的操作空间符合焊接操作需求,并应确保在焊接焊缝时有含量不低于99.99%的惰性气体保护。
5.4.2 不锈钢管道的焊接应采用惰性气体保护焊接。焊接结束后应再用洁净水试压,试压合格后应对管道进行清洗、钝化处理,管道的试验压力应符合现行国家标准《工业金属管道工程施工规范》GB 50235的规定。
5.4.3 引入洁净室(区)的明敷管道应在洁净室间隔完成后安装。
5.4.4 不同的管材、管件或阀门连接时,应使用专用的转换连接件。
5.4.5 阀门安装应便于操作,不得妨碍设备、管道及阀门本身的拆除和检修。
5.4.6 不锈钢管道支架应采用不锈钢管托。塑料管可采用配套的塑料管卡。当塑料管采用金属管卡时,金属管卡与管道之间应采用塑料带或橡胶等软物隔垫。
5.4.7 穿越墙、楼板、吊顶的管道应设套管。管道和套管之间应有密封措施。
5.5 保温
5.5.1 注射用水的热或冷贮存输送系统的管道应保温。
5.5.2 采用热力灭菌方式的纯化水系统的管道宜保温。
5.5.3 洁净区的保温材料应采用不释放纤维和颗粒的材料,保温材料可溶出氯化物、氟化物、硅酸盐及钠离子的含量应符合现行国家标准《覆盖奥氏体不锈钢用绝热材料规范》GB/T 17393的有关规定,并应采用不释放纤维和颗粒的材料作外壳保护。
.
6 站 房
6.1 一般规定
6.1.1 站房位置应根据下列因素,经技术经济比较后确定:
1 靠近工艺用水负荷中心。
2 供水、排水合理。
3 利于设备运输、安装。
4 避免靠近有毒害气体、腐蚀性介质及粉尘产生的场所。
5 不宜布置在变配电站的上方。
6.1.2 站房的规模应根据生产规划所规定的任务,以近期目标为主,并结合远期发展要求,综合分析确定。
6.1.3 站房内接触或可能接触腐蚀性介质的设备表面,应涂衬合适的防护层或采用耐腐蚀材料制作。
6.1.4 站房噪声应符合现行国家标准《工业企业噪声控制设计规范》GB/T 50087的有关规定。
6.2 站房布置
6.2.1 站房布置宜包括设备间和化验室,纯化水制备和注射用水制备宜按区域分开布置。对实施自动化控制的站房应设置控制室。
6.2.2 非独立的站房宜和其他相邻设施隔开。
6.2.3 站房面积应满足设备和管道的布置、安装、操作、维修,以及扩大产能可能性的要求。
6.2.4 站房高度应根据设备高度、安装、吊运,以及站房内通风、采光要求等因素确定。
6.3 设备布置
6.3.1 制水设备宜按工艺流程的顺序以及设备和设施的不同功能布置。
6.3.2 设备布置应留有适当的通道和空间,并应满足正常运行、换料、清洗和维修要求。
6.3.3 同类设备宜相对集中布置。
6.3.4 振动设备应采取减振装置,其噪声应符合现行国家标准《工业企业噪声控制设计规范》GB/T 50087的有关规定。
6.3.5 设备中的阀门、取样口等应排列整齐、便于操作。
6.3.6 酸碱储罐宜布置在室外,寒冷地区可布置在室内。
6.3.7 离子交换柱应相对成列布置,相邻设备间的净距不宜小于0.4m,设备本体为法兰连接时,净距离应适当加大。
6.3.8 电渗析器的突出部分与墙壁净间距不应小于1.0m,与动力设备的净距离不应小于1.5m。电渗析器本体四周应设置排水沟/围堰。
6.3.9 反渗透装置两侧应保持足够的通行宽度,前后应留有足够的空间装卸膜元件。
6.3.10 蒸馏水机及储罐宜靠外墙设置,突出部分与墙壁净间距不宜小于0.5m。
.
7 建筑与结构
7.1 建筑
7.1.2 站房地面、墙壁、顶棚应采用防水、防潮、防霉、易清洗的材料铺设。门窗应采用不易变形材料制成,并应采取防蚊蝇、防尘、防鼠等措施。
7.1.3 对有酸、碱侵蚀的站房地面、门窗、墙柱、围堰或地沟、中和池等建(构)筑物的设计,应符合现行国家标准《工业建筑防腐蚀设计规范》GB 50046的有关规定。
7.1.4 站房应预留能通过设备最大搬运件的安装洞,安装洞可结合门窗洞或非承重墙处设置。
7.1.5 站房通向室外的门应满足安全疏散、便于设备出入的要求。
7.1.6 控制室应设观察窗,观察窗窗台标高不宜高于0.8m,控制室的面积应根据表盘和控制柜的数量确定。控制室宜采用防尘地面,其内墙应光滑平整。
7.2 结构
7.2.2 站房基础类型和地基处理措施应根据地基土质、站房特点、施工条件和运行要求等因素确定。
.
8 公用工程
8.1 电气
8.1.1 除生产工艺明确要求不能中断供应工艺用水外,站房内制水工艺及辅助设施应按三级负荷供电。
8.1.2 站房应有良好的采光及照明,应符合现行国家标准《建筑照明设计标准》GB 50034的规定。
8.1.3 在站房的主要操作地点和通道,宜设置事故照明。
8.1.4 电气设施应满足防潮、防霉及防腐蚀的要求。
8.1.5 站房应设置与其他生产设施内部联系的通信装置。
8.1.6 站房可根据企业规划和生产管理要求,设置视频监视系统。
8.2 给水排水
8.2.1 进入站房的原水管径大小除应满足工艺用水制备的要求外,宜留有发展余量。
8.2.2 管道外表面可能结露时,应采取防结露措施。
8.2.3 站房内的围堰或地沟应能排除积水、便于清洁。
8.2.4 站房的排水汇集管道应采用耐腐蚀的管材。
8.2.5 站房内应设包括消防给水系统及必要的固定灭火装置等消防设施,并应符合现行国家标准《建筑设计防火规范》GB 50016的有关规定。
8.3 暖通空调
8.3.1 站房应保证通风良好,应采用有组织的自然通风。当自然通风不能排除蒸馏水机、工艺用水储罐等的余热时,应设置机械通风。
8.3.2 化验室和控制室宜设置空调和采暖设施。
8.3.3 站房设备间的温度不宜低于15℃。严寒地区的站房在非运行期间,可根据当地情况设置采暖设备。
.
附录A 工艺用水系统的管理和检查、维护
A.1 工艺用水系统的管理
A.1.1 工艺用水系统管道网络图的内容应包括管线、阀门、通气点、排水点、用水点、取样点、清洁点、检验仪表与仪器、水流速度、循环方式等。
A.1.2 工艺用水系统档案,应包括下列内容:
1 工艺用水系统管道网络图。
2 制造、安装厂家的有关资料附件。
3 工艺用水系统工艺规程及标准作业程序(SOP)。
4 工艺用水系统的清洁管理规程及标准作业程序(SOP)。
5 工艺用水质量标准、监测操作规程。
6 记录系统。
7 取样操作规程、检验操作规程等。
8 取样指南、测试程序、验证程序。
9 周期性回顾检查频率、要点。
A.1.3 工艺用水系统日常运行,应符合下列要求:
1 应按操作规程对工艺用水系统实施监控,并应记录各种仪表的数值,同时应定期进行趋势分析。
2 质量控制部门应定期检测水系统的运行状况,并应根据各项指标确定是否需要处理和更换各种组件。
3 应按操作规程消毒、灭菌纯化水、注射用水管道,以及其他供水管路。
4 工艺用水系统停用后再次启动前,应对管路进行清洗。
5 水质检验记录应保存三年。
6 水质检验报告书应附于批生产记录内。
A.1.4 工艺用水系统的现场管理,应符合下列要求:
1 各类管道均应有指明其内容物名称及流向的标识。
2 储水罐等应有内容物名称标识。
3 主要阀门应有开关状态标识。
4 现场宜有工艺用水系统图,操作工应能熟练讲解工艺用水制备的流程。
5 配制清洗液用的容器具、清洁储水罐用的工器具等均应在现场保存。
6 现场操作室不得有积水,卫生状况应良好。
7 用于水质检测的试剂、玻璃器具等均应在现场保存。
A.2 工艺用水系统的检查、维护
A.2.1 工艺用水系统的检查项目以及合理的督察计划,应包括下列内容:
1 所有取样点的取样和监测计划。
2 监测中需要报警和采取措施的参数设定。
3 监测结果和趋势评估。
4 对系统最近一次年度检查结果的审查。
5 对最后一次检查后系统的所有变更进行审查,并检查是否实施了变更控制。
6 审查所记录的变动以及对变动进行过的调查。
7 对系统状态和条件的全面检查。
8 审查维护、失败和维修记录。
9 检查关键仪器设备的校审和校准。
10 对于新系统还需检查系统性能确认、运行确认、安装确认文件。
A.2.2 工艺用水系统应按标准作业程序(SOP)维护,并应包括下列内容:
1 关键仪表的校验计划。
2 系统各部件的维护频率。
3 特定作业的标准作业程序(SOP)。
4 对设备备件的控制。
5 维修指令和计划的发布。
6 在维修工作完成后,系统投入使用前的审查和批准。
7 维护过程中的记录,对偏差的审核、评估及纠正措施等。
.
附录B 纯化水、注射用水系统确认要求
B.1 纯化水、注射用水系统确认的内容
B.1.1 设计确认(DQ)应包括检查设计的完整性,检查设计满足用户需求、生产工艺需求的符合性,检查设计满足GMP要求和产品质量标准的符合性。
B.1.2 安装确认(IQ)应包括文件和图纸确认,系统图和布置图的确认,设备/部件(包括备件)确认,仪器仪表确认,控制系统硬件确认,控制系统软件确认,与产品接触材质确认,死角检查,焊接文件确认,排放能力的确认,压力测试的确认,脱脂清洗和钝化的确认,公用设施确认。
B.1.3 运行确认(OQ)应包括系统验证仪器校准的确认,人机界面的确认,运行功能的确认,报警和联锁的确认,关键操作参数(包括运行和消毒方式相关参数)测试,制备系统单元操作的确认,储存分配系统的确认,水质离线检测。
B.1.4 性能确认(PQ)应在安装确认(IQ)及运行确认(OQ)合格的前提下,检查工艺用水系统满足生产要求的符合性,以及检查送水口、回水口、各使用点工艺用水的各项相关指标满足工艺用水质量标准的符合性,并应确保系统稳定连续地生产出合格的水,以及确认清洗消毒周期。
纯化水、注射用水系统性能确认过程中,应按系统标准操作程序、维护保养程序、取样程序、检验规程和质量标准进行操作和判定。出现个别取样点水质量不符合标准的结果时,应按异常情况处理程序进行处理。
B.2 纯化水、注射用水确认文件目录
B.2.1 纯化水、注射用水系统的确认文件应包括设计确认的方案和报告、安装确认的方案和报告、运行确认的方案和报告、性能确认的方案和报告。
B.2.2 纯化水、注射用水系统的确认,可分解为制备系统的确认、储存和分配系统的确认。
B.2.3 设计确认,文件目录可包括下列内容:
1 批准页。
2 目的。
3 范围。
4 职责。
5 参考标准。
6 系统描述。
7 确认项目可包括下列内容:
1)人员的确认;
2)设计文件的确认;
3)设计参数和标准的确认;
4)设备/部件的确认;
5)仪表的确认;
6)施工要求的确认;
7)系统功能的确认。
8 偏差报告。
9 附件清单。
10 执行结果的审核和批准。
B.2.4 安装确认,文件目录可包括下列内容:
1 批准页。
2 目的。
3 范围。
4 职责。
5 参考标准。
6 系统描述。
7 测试项目可包括下列内容:
1)人员的确认;
2)文件的确认;
3)系统图和布置图的确认;
4)设备/部件的确认;
5)仪表的确认;
6)材质和表面抛光的确认;
7)主要设备和部件的卫生型结构的确认;
8)死角的确认;
9)焊接文件的确认;
10)排放能力的确认;
11)压力测试的确认;
12)脱脂清洗和钝化的确认;
13)公用设施的确认;
14)控制系统硬件组成的确认;
15)控制系统软件配置的确认。
8 偏差报告。
9 附件清单。
10 执行结果的审核和批准。
B.2.5 运行确认,文件目录可包括下列内容:
1 批准页。
2 目的。
3 范围。
4 职责。
5 参考标准。
6 系统描述。
7 测试项目可包括下列内容:
1)人员的确认;
2)验证仪器校准的确认;
3)人机界面的确认;
4)运行功能的确认;
5)报警和联锁的确认;
6)设备操作参数的确认;
7)使用点峰流量的确认;
8)消毒/灭菌过程的确认。
8 偏差报告。
9 附件清单。
10 执行结果的审核和批准。
B.2.6 性能确认,文件目录可包括下列内容:
1 批准页。
2 目的。
3 范围。
4 职责。
5 参考标准。
6 系统描述。
7 测试项目可包括下列内容:
1)人员的确认;
2)水质标准和取样点清单;
3)取样标准操作规程的确认;
4)第一阶段,密集取样和水质测试;
5)第二阶段,密集取样和水质测试;
6)第三阶段,日常取样和水质测试。
8 偏差报告。
9 附件清单。
10 执行结果的审核和批准。
附录C 工艺用水检测仪表选用要求
C.0.1 工艺用水检测仪表选用应符合下列要求:
1 工艺用水系统仪表、控制水平和方式,应根据生产规模、生产设备自动化水平、管理水平、工艺用水系统设备和检测要求,以及自动化设备元件供应情况等因素经技术经济比较确定。
2 工艺用水检测仪表应具有医药工艺用水工艺流程要求的可靠性和检测精度。
3 工艺用水应选择符合卫生要求、便于更换的仪表。与严格限制微生物的工艺用水直接接触的传感器应为卫生级结构。非卫生级仪表宜用于原水和预处理系统。
4 仪表接触工艺用水的表面应光滑,并应采用与工艺用水兼容的材料制造。
5 仪表应满足在线灭菌和耐腐蚀要求。
6 设计中采用的仪表不得选用未经工业鉴定的试制仪表。
C.0.2 温度仪表应符合下列要求:
1 就地温度仪表应选用卫生级双金属温度计,刻度盘直径宜选用100mm。
2 要求以标准信号传输的场合,应采用温度变送器。在满足设计要求的情况下,可选用测量和变送一体化的温度变送器。
3 温度传感器应拆装方便,并应便于清洗、维护,同时应能耐高温蒸汽清洗消毒,稳定性应好,测量精度应高。
4 检测元件及保护套管,应根据温度测量范围、安装场所等条件选择,热电偶可用于一般场合;热电阻可用于精确度要求较高的场合。热电阻、热电偶的连接方式应选用卫生级连接。卫生级连接不应产生死角或无法排空的区域。
5 检测元件保护套管材质应与相关工艺用水设备或管道材质一致,表面光洁度应高。
C.0.3 压力仪表应符合下列要求:
1 就地压力仪表应选用卫生级隔膜压力表,刻度盘直径宜选用100mm。
2 当采用标准信号传输时,应选用卫生级隔膜型压力变送器。
3 卫生级隔膜压力表或隔膜型压力变送器结构和材料应符合卫生要求,表面光洁度应高,应无死角,并应便于清洗、维护、安装和拆卸。
4 卫生级隔膜压力表或隔膜型压力变送器应能耐高温蒸汽清洗消毒。
5 卫生级隔膜压力表或隔膜型压力变送器稳定性应好,测量精度和可靠性应高。
C.0.4 流量仪表应符合下列要求:
1 流量仪表应选用卫生级流量计。
2 卫生级流量计的材质应与工艺用水设备或管道材质一致,表面光洁度应高;应防止测量介质残余物在测量管中的堆积,测量管道内应无可移动部件。
3 卫生级流量计应在使用过程中不易被污染,并应便于清洗、维护、安装和拆卸。测量精度应高,结果应可靠。
4 卫生级流量计应能耐高温蒸汽清洗消毒。
C.0.5 液位仪表应符合下列要求:
1 液位仪表应选用卫生型液位计。
2 液位计的材质应与工艺用水设备的材质一致,内外壁表面应采用抛光处理,应无死角,并应易清洗,同时应适合容器内液体介质的液位、界位测量。
3 测量范围应大,不应受储槽高度限制,指示机构与被测介质应完全隔离。
4 液位计应结构简单、可靠、安全,维护费用低,并应便于清洗、维护、安装和拆卸。
5 当采用自动控制时,除现场指示外,还可配置远传变送器、报警等功能。
C.0.6 总有机碳(TOC)测定仪应符合下列要求:
1 总有机碳(TOC)测定仪最低检出限为每升含碳不应高于0.050mg/L(50ppb)。
2 总有机碳(TOC)测定仪应符合定期的系统适用性测试要求。
3 总有机碳(TOC)测定仪监测方法应能区分无机碳。
本规范用词说明
1 为便于在执行本规范条文时区别对待,对要求严格程度不同的用词说明如下:
1)表示很严格,非这样做不可的:
正面词采用“必须”,反面词采用“严禁”;
2)表示严格,在正常情况下均应这样做的:
正面词采用“应”,反面词采用“不应”或“不得”;
3)表示允许稍有选择,在条件许可时首先应这样做的:
正面词采用“宜”,反面词采用“不宜”;
4)表示有选择,在一定条件下可以这样做的,采用“可”。
2 条文中指明应按其他有关标准执行的写法为:“应符合……的规定”或“应按……执行”。
引用标准名录
《建筑设计防火规范》GB 50016
《建筑照明设计标准》GB 50034
《工业建筑防腐蚀设计规范》GB 50046
《工业企业噪声控制设计规范》GB/T 50087
《工业金属管道工程施工规范》GB 50235
《生活饮用水卫生标准》GB 5749
《覆盖奥氏体不锈钢用绝热材料规范》GB/T 17393
《城市给排水紫外线消毒设备》GB/T 19837
《热压式蒸馏水机》JB 20029
《多效蒸馏水机》JB/T 20030
